高小杰 wrote:
以色列不良反應統計!(恕刪)
因為這個病毒的設計也相當歹毒 , 正好對抗腎素-血管收縮素-醛固酮系統(renin-angiotensin-aldosterone system, RAAS)中 , 舒張血管降血壓 的機制
這個病毒所選擇的受體是 ACE2 (angiotensin-converting enzyme 2) 血管收縮素轉化酶 , 是一種跨膜的結構域及細胞通道。
血管收縮素II具有高效的收縮血管作用,從而使血壓升高。
ACE2通過轉化"血管緊張素 II"和增加 Ang(1-7)血管擴張,來拮抗相關血管緊張素轉換酶(ACE)的活性。
當病毒上的棘蛋白結合ACE2受體後,就能由此通道進到細胞內大量增生,導致感染,同時還會暫時抑制ACE2原本穩定血管收縮與抗發炎反應 ,ACE2表現量的下降與數種心血管疾病有相關性。
當疫苗 摹擬 病毒的S蛋白 , 去嵌入 ACE2受體 時 , 同時還會抑制ACE2原本抗血管收縮(舒張)與抗發炎反應 ,這對於原本有心血管疾病相關病患相當不利 , 打疫苗反而會引發"心血管疾病"發作 。
美國曾經收集2019大流行前的血漿樣本, 發現大流行前的血清, 已經存在對 SARS-CoV-2 的交叉反應抗體, 推測是之前感染類似普通感冒OC43,NL63、HKU1等輕微症狀冠狀病毒親戚 ,如同牛痘對人痘(天花)有交叉反應 , 先前其它種類的冠狀病毒感染對 SARS-CoV-2這個親戚也產生了交叉免疫反應。
有交叉保護這能解釋是為何 有80%的人無症狀感染 ? 輕症? 無交叉保護會重症死亡?
老年人缺乏 交叉反應性 T 淋巴細胞 , 之前感染人類冠狀病毒 OC43 和 NL63, 難以對 SARS CoV-2有保護, 解釋了60 歲以上的老年人為何佔重症死亡率95% 以上。
但是如同登革熱 , 若二次接觸抗原, 可能發生"抗體依賴增強作用",Antibody-dependent enhancement(ADE)?
以及immune complexes免疫複合體 , 與補體結合後, 會引發自體免疫(第三型hypersentavity)?
若作用於血管上皮, 主動脈剝離合併心包塞填,懷疑不只血管無法舒張,怕還有免疫複合體immune complex,
這都造成苗開發的困難
結合ACE2 的S蛋白是天然的嗎 ? 是可以人工切換,轉換為不同的S蛋白
我們怎麼能這麼確定?
因為 武漢病毒研究所的研究基金是來自 美國國立衛生研究院 (NIH) 下屬的國家過敏和傳染病研究所 (NIAID) 的資助。
原本撥款給紐約生態健康聯盟的主席 , 英國科研者Daszak 博士,承包商 Daszak 博士又將其轉包給了武漢病毒研究所的石博士。由於提供資金的撥款提案是公共記錄的問題,必須向美國國會具體說明她計劃用這筆錢做什麼。因此留下了書面紀錄。
書面紀錄可知
武漢病毒研究所的實驗室,一直在做基因工程冠狀病毒去攻擊人體細胞的工作。稱之為"功能增強性研究gain-of-function experiments"
把一個不會感染人的病毒, "功能增強性gain-of-function "後去攻擊人體
2018 和 2019 財年撥款的摘錄如下。“CoV”代表冠狀病毒,“S 蛋白”是指病毒的刺突蛋白。
“對 CoV 種間傳播的測試預測。宿主範圍的預測模型(即出現潛力)將使用反向遺傳學、假病毒和受體結合分析,以及來自不同物種和人源化小鼠的一系列細胞培養物的病毒感染實驗進行實驗測試。”
“我們將使用 S 蛋白序列數據、感染性克隆技術、體外和體內感染實驗以及受體結合分析來檢驗 S 蛋白序列中百分比差異閥值, 以預測溢出(spillover)潛力的假設。”
用非技術語言來描述上列文字,石博士打算著手創造對人類細胞具有最高感染力的新型冠狀病毒。她的計劃是採用編碼刺突蛋白的基因,這些基因對人類細胞具有從高到低的各種可測量的親和力。她會將這些刺突基因一個一個地插入到許多病毒基因組的骨架中(“反向遺傳學”和“傳染性克隆技術”),從而創造出一系列"嵌合病毒"。然後將測試這些嵌合病毒攻擊人類細胞培養物(“體外”)和人源化小鼠(“體內”)的能力。這些訊息將有助於預測病毒“溢出spillover”的可能性,即冠狀病毒從蝙蝠傳播到人類。
檢索相關論文發現,他們使用一種 HIV 假病毒來表達 7 種蝙蝠 b-ACE2 受體,並將它們的結合人類 h-ACE2 受體特性,以便選擇最好的受體,以進一步優化 SARS 樣冠狀病毒結合人體細胞的能力。 他們還發現,一些蝙蝠 ACE2 受體與人類 ACE2 受體非常接近。 這項研究提供了一個模型系統,在 2005 年至 2013 年間對中國蝙蝠種群的大量調查中 , 選擇已經用於測試的最具傳染性的 SARS-CoV 樣病毒。(Xu L 等,2016)。 這些病毒可能通過 ACE2 受體感染人類。 2012-2015 年間發現了更多新病毒(Lin etal,2017)。
是 石正麗 發表在《Nature》 volume 579, pages270–273 (2020)的論文自己說的

石正麗 說 a short region of RNA-dependent RNA polymerase (RdRp) from a bat coronavirus (BatCoV RaTG13)—which was previously detected in Rhinolophus affinis from Yunnan province—showed high sequence identity to 2019-nCoV.
來自蝙蝠冠狀病毒 (BatCoV RaTG13) 的 RNA 依賴性 RNA 聚合酶 (RdRp) 的一小段區域(之前在雲南省的 Rhinolophus affinis 中檢測到)顯示出與 2019-nCoV 的高度序列同一性。
這是該文自己表達的 RaTG13 是 2019-nCoV 最近親屬 的基因樹

for all sequences—RaTG13 is the closest relative of 2019-nCoV
對於所有序列——RaTG13 是 2019-nCoV 的最近親屬
for all sequences—RaTG13 is the closest relative of 2019-nCoV and they form a distinct lineage from other SARSr-CoVs
對於所有序列——RaTG13 是 2019-nCoV 的近親,它們形成了與其他 SARSr-CoV 不同的譜系
全部都是 石正麗自己說的
有沒有做成功? 由過去武漢病毒研究所 發表過的論文可以看出
法國世界報 , 批漏了 石正麗 指導的研究生 的三篇論文
https://www.rfi.fr/cn/中国/20210527-covid-19溯源-武汉病毒研究所未发表的三篇论文遭披露-事故假设被重提
第一篇
提到了和 新冠SARS-2病毒 有96%相似, 在雲南礦坑發現的RaTG13 (Ra4991)病毒

其中一位喻萍的碩士論文,「蝙蝠SARS樣冠狀病毒的地理進化研究」研究了當時2012年,從雲南墨江通關鎮這個地方,所分離的一些病毒株。她實際上有對四個病毒株,來自雲南墨江的病毒株進行全基因組的測序,這個在石正麗的所有的文章中,沒有這麼完整的說明過。
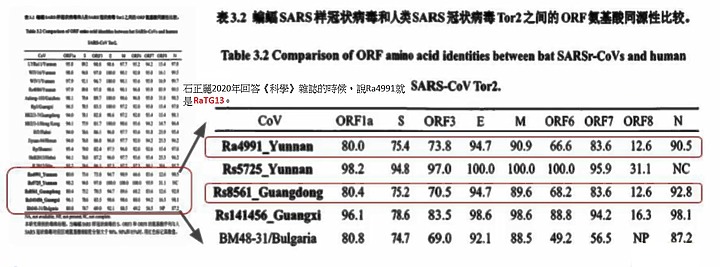
石正麗在2020年回答《科學》雜誌的時候,她說Ra4991就是RaTG13。可是這一次《世界報》,比較研究生論文發表出來的序列,和RaTG13這二個序列之後,發現一個非常有意思的事情,二者用來感染人的那部分的這種蛋白,差異有多大,1%~1.5%,科學解釋這樣的差異需要進行十次到十五次的變異才能達到這樣的變化,可是石正麗親口講,這二個是同一個病毒? 在實驗室內"連續繼代"才造成差異嗎 ?
第二篇 武漢病毒實驗室早就具有 改變病毒S蛋白 為 ACE2 的能力
如果這個野生病毒株沒有接合 ACE2 受體的能力 ? 那就給它一個 ACE2受體能結合的蛋白
2008年Wuze Ren等人在病毒學期刊上, 成功展示了在蝙蝠 SARS 樣病毒和人類 SARS 病毒之間交換 RBD 的技術能力:“......
發現最小插入區(氨基酸 310 至 518)足以將 SL-CoV S 從非 ACE2 結合轉化為與人類 ACE2 結合,表明 SL-CoV S 與 SARS-CoV S 在很大程度上兼容蛋白質的結構和功能。
J Virol. 2008 Feb; 82(4): 1899–1907.
Difference in Receptor Usage between Severe Acute Respiratory Syndrome (SARS) Coronavirus and SARS-Like Coronavirus of Bat Origin▿
(Wuze Ren , 等人,中國科學院武漢病毒研究所2008 年)。
Wuze Ren,中文 : 任武澤,中國科學院武漢病毒研究所石正麗研究員2004~2007年指導的博士研究生,曾獲2007年中國科學院院長獎學金優秀獎、湖北省優秀博士學位論文獎。
2008年石正麗的博士生任武澤 , 成功展示了在蝙蝠 SARS 樣病毒和人類 SARS 病毒之間交換 RBD 的技術能力:“......
發現最小插入區(氨基酸 310 至 518)足以將 SL-CoV S 從非 ACE2 結合轉化為與人類 ACE2 結合,表明 SL-CoV S 與 SARS-CoV S 在很大程度上兼容蛋白質的結構和功能。
法國世界報批漏 这三篇论文中,2017年的博士论文「蝙蝠SARS樣冠狀病毒的反向遺傳學系統的建立及ORFX功能研究」最顶尖;它利用了嵌合病毒构建技术,即一种 "复制粘贴"的方式。中国研究人员的目标之一是测试不同冠状病毒对几种类型的人类或动物细胞的感染性,而这取决于嫁接在同一病毒骨架上的「編碼基因」。

论文作者曾磊平写道:"为了估计类似SARS的蝙蝠冠状病毒对人类的潜在威胁,我们从不同的冠状病毒毒株中选择了12个S(即尖峰编码)基因,并将它们插入WIV1(另一种冠状病毒)的基因组框架中,作者说,"我们成功地获取了其中四个,分别将其命名为Rs4231、Rs4874、Rs7327和RsSHC014病毒株。"
石正麗的實驗室已經展示, 任何冠狀病毒都能換上 RBD 區的編碼 ,就有ACE2的強結合 ?
有?或是沒有 ACE2結合力 ? 完全都是可以在實驗室內"複製貼上" , 是完全可以自行控制的, 不必天然病毒
SHC014 又出現了 ?
再對照回到 石正麗於 2015年 發表於 Nature的重組嵌合病毒(稱為 SHC014--MA15)?
石正麗博士與北卡羅來納大學著名的冠狀病毒研究人員拉爾夫·S·巴里克 (Ralph S. Baric) 合作。他們的工作重點是增強蝙蝠病毒攻擊人類的能力,以“檢查正在傳播的蝙蝠 CoV [冠狀病毒] 的出現潛力(即感染人類的潛力)。”
為實現這一目標,他們於 2015 年 11 月創造了一種新型病毒,採用 SARS1 病毒的骨架並將其刺突蛋白替換為來自蝙蝠病毒(稱為 SHC014-CoV)的刺突蛋白。這種人造病毒能夠感染人類呼吸道的細胞,至少在針對此類細胞的實驗室培養物進行測試時是如此。
Nature Medicine 的這一篇報告 , 就提到它們還有 編碼新型,人畜共患的冠狀病毒刺突蛋白的嵌合病毒-(SHC014-MA15)
《A SARS-like cluster of circulating bat coronaviruses shows potential for human emergence》

新的人畜共通的的嵌合病毒 (SHC014-MA15)是將SARS病毒的刺突蛋白 ,替換為來自蝙蝠病毒(稱為 SHC014-CoV)的刺突蛋白 ?
對照曾磊平的論文 , 是將基因(即尖峰编码)插入WIV1(另一种冠状病毒)的基因组框架中 ? 去得到 SHC014 ?
原本以為是 天然蝙蝠病毒的 SHC014-CoV ? 卻是曾磊平选择了12个S(即尖峰编码)基因,并将它们插入WIV1另一种冠状病毒, 所變出來的實驗室嵌合病毒?
石正麗 拿了這種嵌合病毒 SHC014-CoV 再去和SARS嵌合? 再變出 (SHC014-MA15)人畜共通的的嵌合病毒 ?
石正麗 在 Nature Medicine 的這一篇報告 , 就昭告全世界, 做出實驗室合成出來的病毒 !
沒想到她拿來嵌合SARS的 , 就已經是嵌合病毒
英國倫敦聖喬治大學的腫瘤學教授達格利什(Angus Dalgleish) 和挪威病毒學家索倫森(Birger Sørensen)
對於石正麗發表過的四篇一序列相關研究論文的解釋
對相關文獻的全面回顧表明,大量直接相關的 “功能增強 gain of function”已經進行了研究。 有四項研究特別值得注意。 它們以兩種方式聯繫在一起:在科學上,第三次和第四次建立在第一次和第二次結果的基礎上,所有四個試驗在整個機構和人員上有連續性。 武漢病毒研究所是所有這些項目的主要合作者,石正麗博士是其中之一,她是研究所最有經驗的病毒學家和蝙蝠專家,貫穿所有關鍵研究項目的共同主線。
1. 2008 年,Shi石博士所在的團隊之研究導致 SARS-CoV-2 確切功能的項目, 是兩個相關聯的”功能增強”先期計劃 ,包括通過 SADS 發現的功能和
如上所述,可能在 2018 年的研究中進行了現場測試。 2008年任武澤等人項目成功展示了在蝙蝠 SARS 樣病毒和人類 SARS 病毒之間交換 RBD 的技術能力:“......
發現最小插入區(氨基酸 310 到 518)足以將 SL-CoV S 從非 ACE2 轉化
與人 ACE2 結合,讓 SL-CoV S同時在結構和功能少上, 很大幅度與 SARS-CoV S 蛋白相容。
這些顯著的發現 ,在病毒起源、病毒重組 和 轉換宿主 被討論了”(Ren 任等人,2008 年)。Shi石博士是該序列中第二篇論文的主要作者,(Hou et al, 2010) 和和第三篇的資深中國作者 (Menachery et al, 2015) 合著。她也是第四篇文獻其中一個合著者(Zhou P. et al, 2018)
2. 2010年武漢病毒所“特殊病毒”科的科學家與國際合作者共同開展從事“增強功能實驗” ,以增加 SARS-CoV 對人類的傳染性。
他們使用一種 HIV 假病毒來表達 7 種蝙蝠 ACE2 受體,並將它們的結合人類 ACE2 受體特性,以便選擇最好的受體,以進一步優化 SARS 樣冠狀病毒結合人體細胞的能力。 他們還發現,一些蝙蝠 ACE2 受體與人類 ACE2 受體非常接近。 這項研究提供了一個模型系統,在 2005 年至 2013 年間對中國蝙蝠種群的大量調查中 , 選擇已經用於測試的最具傳染性的 SARS-CoV 樣病毒。(Xu L 等,2016)。 這些病毒可能通過 ACE2 受體感染人類。 2012-2015 年間發現了更多新病毒(Lin etal,2017)。
3. 2015年武漢病毒所“特殊病毒”科的科學家,與北卡羅來納大學教堂山分校為多數的團隊一起聯合進行”增強功能實驗”。 他們操縱蝙蝠病毒創造了一種適應小鼠的新型嵌合病毒SHC014-MA15 , 能在人類上呼吸道細胞(2B4 Calu-3 - Chapel Hill 提供的細胞系)上增殖:(“2b 組病毒在野生型骨架中編碼了 SHC014 棘突蛋白Spike可以有效得利用多個同源直系 ACE2受體,在原代人體氣道細胞中有效複製,並在體外接種效價達到與流行毒株SARS-CoV相當的效果”)。我們建議在進一步調查中, 高度優先從教堂山分校 精準得確認實驗室記錄了 2B4 Calu-3 的確切捐贈出處。
我們注意到這裡描述的 , 提供冠狀病毒材料的武漢首席科學家,是Zheng-Li Shi 石正麗博士(“提供了SHC014 刺突序列和質粒”)。
事實上,這正是 SARS-CoV-2 的特性。複製嵌合病毒在教堂山分校進行的鼠體內實驗, 和團隊的預期相反, 小鼠肺顯示出顯著的發病機制(預計 SHC014-MA15 等嵌合病毒的產生不會增加致病性”)。 Menachery 等人據報導,可能很難開發出針對 SHC014-MA15 的疫苗。因此,我們可以看到,2015 年實驗推進了 2010 年的工作,通過在動物試驗中完善一種病毒來感染人類上呼吸道。 2015 年的作者很清楚他們創造的嵌合病毒非常危險,因為他們討論了這個事實。在他們研究的機會/成本中,他們建議
“在為未來新出現的病毒提供準備時,必須在以下情況下考慮這種方法”
美國政府要求暫停 增強功能 (Gain of Function) 研究”(此後已取消)。他們也推測“審查小組可能認為類似的研究風險太大而無法進行,因為在
不能排除哺乳動物模型。” 這個實驗肯定是創造了具有針對人類上呼吸道的極高傳染性潛力的 “嵌合病毒”。然而一個令人驚訝的觀察是 ,該論文指出,該研究聯盟有權繼續進行這項研究。看起來針對這種嵌合病毒的”增強功能”工作仍在繼續。我們從論文作者中推斷出這是在武漢病毒研究所完成的。
4. 如前所述,2018 年,石博士的同事Peng Zhou 周鵬和其他人一起調查了一次與廣東省一起致命的豬急性腹瀉綜合徵(SADS)有關的冠狀病毒爆發。這篇論文涉及到仔豬在腸道中有一個組織特異性感染位點,並且證實了蝙蝠 Covid 的性質, 這種新的 SADS 作為致病因子得到了證實。 25,000 頭小豬死亡。然而,真正有趣的 ,這項研究的一部分報告說,為了識別 SADS CoV 使用的受體,研究了已知的冠狀病毒宿主細胞受體: 血管緊張素轉化酶 2 (ACE2)、氨基肽酶 N (APN) 和二肽基肽酶 4 (DPP4)。這些受體都不起作用。但在他們的論文中,作者間接地透露 它們以早先提出的方式表達和測試新受體的能力。重新組合的模式 在 2010 年的工作中得到了證明和報告。因此很明顯,SADS 是一種利用新組織特異性結合域的冠狀病毒 CoV 感染;除了說它不是最著名的三個中的任何一個 , 作者沒有提供關於病毒在仔豬中使用哪種受體的暗示。我們在上面補充了“已扣除額deduction”。豬隻免疫力系統當然與人類非常相似。
現在回想一下 Menachery V.D 等人在 2015 年的研究表明,他們的嵌合病毒 SHC014-MA15 可以相反於他們的預測,非常成功地感染來自細胞系 2B4 Calu-3 的原代人上呼吸道上皮細胞 (HAE)。考慮到這一點,我們接下來觀察到,在 Covid-19 大流行中,感染早期的一個充分報告的症狀是味覺喪失、頭痛和喉嚨痛。我們在 QRBD 文章中詳細討論了這個問題。但總結一下:在2015 年在一篇研究綜述(Workman 等人,2015 年)中討論了苦/甜味受體以及這些受體所起的作用 介導氣道免疫功能。他們得出這樣的結論:“在過去的幾年裡,味覺受體已經出現作為調節哺乳動物呼吸道先天免疫防禦的關鍵參與者。其中的幾種氣道細胞類型,包括纖毛上皮細胞、孤立的化學感應細胞和支氣管平滑肌細胞,均顯示利用味覺受體的化學反應特性。”
因此,我們假說 Spike 的重建歷史病因學如下:
2008 年,Zheng-Li Si 石正麗博士和 WIV 同事成功展示了,在蝙蝠 SARS 樣病毒和人類 SARS 病毒RBD 之間交換 RBD 的技術能力。←將冠狀病毒換上一個能感染人的S蛋白
在此基礎上,2010 年的工作(Hou 等,2010)完善表達了人體細胞上受體的能力。在這些基礎上,核心的”增強功能”工作支撐了發生了 SARS-CoV-2,攜帶 WIV 刺突和質粒材料成功地與 UNC 教堂山分校提供的人類上皮細胞結合。這項工作(Menachery 等人)產生了一種高度傳染性的嵌合病毒,該病毒針對人類上呼吸道進行了優化。←將冠狀病毒和SARS嵌合成另一種新病毒
為了支持這一假設,Lu (Lu et al, 2020) 和 Jia (Jia et al, 2020) 目前都有,在
2020 年 1 月和 4 月,表明 SARS-CoV-2 具有蝙蝠 類SARS病毒的骨架,但攜帶來自人類 SARS病毒 的 RBD 。
和我們一樣,Zhan等人也注意到從第一個分離株開始對人類的異常適應。在 2015 年的教堂山工作中,僅討論了 ACE2 受體。然而,2018 年 Zhou P. 等人展示了複製其他相同基因受體(如 APN 和 DPP4)的能力,並將這些受體與鑑定的(腸道)組織特異性 SADS-CoV 進行測試和比較。
然後,在 2019-20 Covid-19 大流行中,出現出大量 苦/甜受體受損的症狀的
報導。綜上所述,這意味著通過採用剛剛推導出的 2015 年之後獲得的見解,進一步優化 2015 年嵌合病毒 ,額外結合,例如氣道上皮受體苦/甜特異性受體/輔助受體 。這將有助於解釋與 SARS-CoV-2 相關, 卻令人費解的高傳染性和病理學,因此也有助於解釋其傳播的流行病學。←讓冠狀病毒S蛋白帶正電, 能靜電吸附上帶負電的人體細胞
傳統上 , 病毒 S蛋白 嵌入 人類ACE2受體 → 造成感染的模式 ,但這個SARS-2病毒還有 『靜電吸附』的能力 , 不必受體也能感染
病毒 S蛋白 嵌入 人類ACE2受體的感染模式, 以插頭 VS 插座 來解釋
抗原 →嵌入 受體
什麼樣的抗原 → 引發特定什麼樣的抗體
台灣 A 型插頭是 兩個平行的金屬片直插頭 , 接上的NEMA 1–15規格 直縫的插座
歐洲C 型插頭具有兩個直徑為4毫米(0.157英尺)的圓頭探針 , 是插入 CEE 7/16 規格 的雙孔插座 ,並無法插入 NEMA 1–15規格 直縫的插座 。
買了IKEA 的插座安全蓋 , 如同"抗體" , 擋住了插頭(病毒) , 病毒就進不了插座(人體受體)
"不同的病毒 , 有不同的抗原 → 產生 特異性抗體
但是 , 象印熱水瓶的電線插頭是帶磁性 , 接近就會吸上水瓶上的插座 , 不需要準確的插頭 對上 插座
這個病毒 的S蛋白, 被嵌入4個帶正電荷的氨基酸 , 能吸附上帶負電的受體, 不一定需要 ACE2 受體
這是造成打過疫苗"突破性感染"的主因 , 也因此造成非ACE2受體的味覺細胞也會被"靜電吸附"而感染上
剛開始不能講明 , 不能自己承認在S蛋白上動了手腳 , 在上面增加了 "正電荷" ?
所以 , 用心良苦創造出一個 "氣溶膠" 的名詞 ?
來說明這不只是 "飛沫" , 還能黏上去
剛開始沒有人能了解 , 這冠狀病毒不是飛沫傳染嗎? 怎麼會是空氣傳染 ?
由於ACE2受體 , 造成如同登革熱 , 二次接觸抗原, 可能發生抗體依賴增強作用,Antibody-dependent enhancement(ADE)?
以及immune complexes免疫複合體 , 與補體結合後, 會引發自體免疫(第三型hypersensitivity)?
這都造成苗開發的困難
由於這個病毒受體為ACE2, ,當疫苗模擬了病毒的S蛋白去結合了ACE2 , 就會暫時抑制了ACE2舒張血管降血壓的功能 。而所有的疫苗 , 包括AZ ,BNT, Moderna 才會都發生了心血管的不良作用
打過疫苗, 因為受體ACE2被嵌合, ACE2無法轉換Ang1-7,以反向作用去舒張血管, 只要感覺胸悶, 血壓變化及心跳變慢變快都要趕快就醫 。
疫苗的副作用 正好 反證了 病毒的受體是ACE2 , ACE2受體結合了病毒, 造成了磨紗樣病毒性肺炎病變